水分解のための新規光触媒材料の開発
図1のような光エネルギーを用いて水を分解する反応(H2O → H2 + 1/2O2)は、光合成のもっとも基礎的な反応であり、学問的に興味が持たれます。また、これらは、ギブスの自由エネルギー変化が非常に大きな反応であり、光エネルギーの化学エネルギーへの変換という観点からも重要な反応です。さらに、この反応で得られた水素は、クリーンエネルギーや化学工業原料として非常に有用です。そこで当研究室では、図のように、半導体を用いた不均一系光触媒を用いた水分解を行っています。
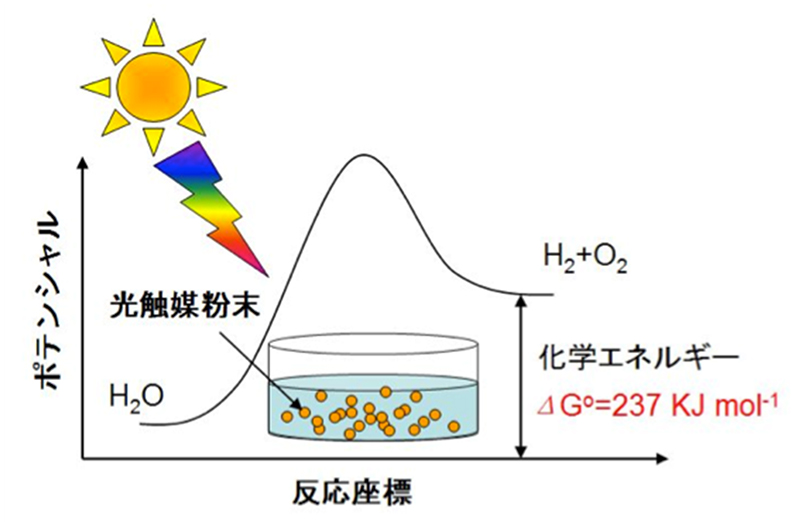
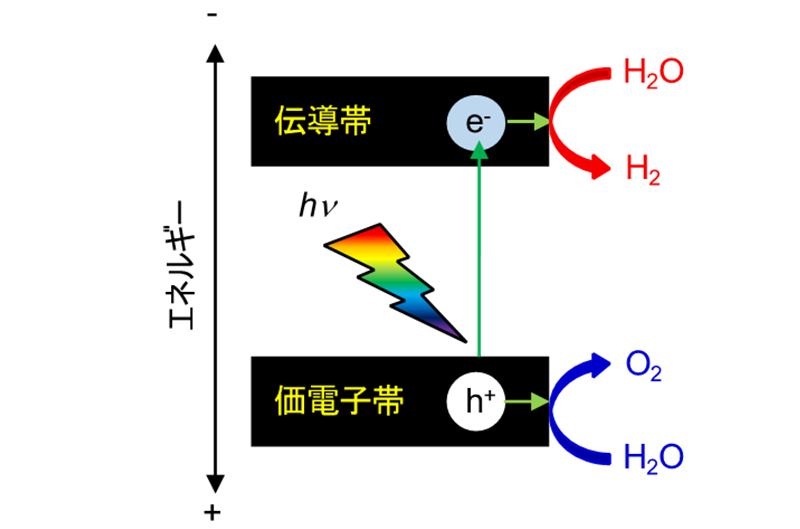
図2に不均一系半導体光触媒による水の分解反応の原理を示します。半導体にバンドギャップ以上のエネルギーの光を当てると、価電子帯の電子が伝導帯へと励起されます。このように励起された電子は、水を還元し水素を生成します。一方で価電子帯に形成されたホールは、水を酸化し酸素を生成します。このようにして光触媒による水の分解反応が進行します。この反応は一見簡単そうに見えますが、実際にはいろいろな要因がかかわってくるので、非常に困難です。
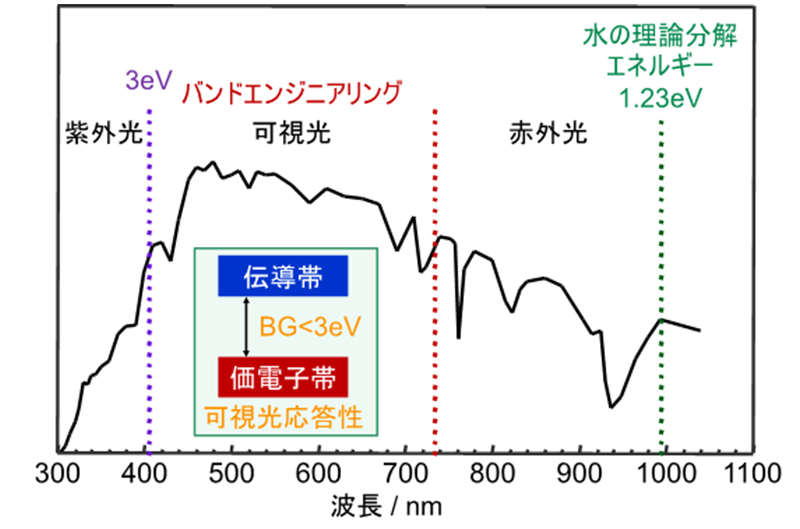
ここで、図3に示すように、太陽光には赤外線から紫外線まで幅広い波長の光が混ざっており、多くの光子を吸収できる光触媒の開発が重要です。このため、効率よく太陽光を使ってこの反応を行うには、長波長の光に応答する活性の高い光触媒の開発が望まれます。このような観点から太陽光を効率よく使って水分解を行うための光触媒の開発がさかんに行われています。しかし、効率的に満足できる光触媒はいまだありません。そこで、水の光分解反応、すなわち人工光合成に高い活性を示す光触媒を開発することを目的として、研究室独自の設計指針に基づいて研究を行っています。さらに、温和な条件下でのセラミックス合成という観点から,新たな光触媒のソフトプロセス合成法の確立を行っています。また、固体表面反応や光電子移動などの学術的観点から、計算科学も取り入れながら光触媒サイエンスとしての研究を行っています。以下に具体的なテーマを示します。
新規光触媒材料の開発
当研究室では、表1に示すような光触媒ライブラリーを構築してきました。これらの中でも、タンタル系複合酸化物の多くが、高効率な水分解活性を示すことを見出してきました。
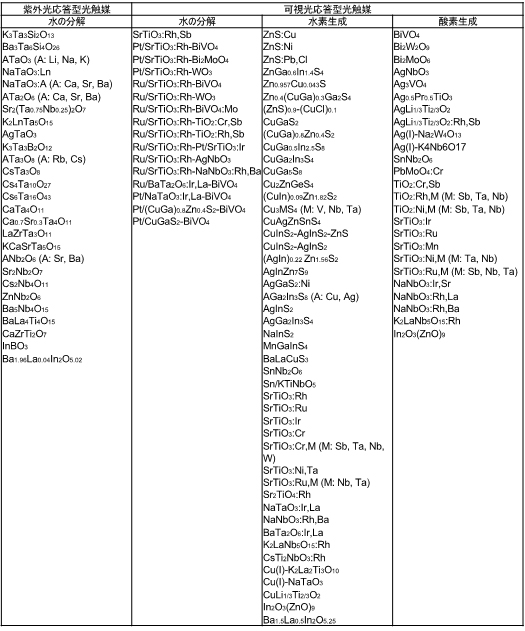
図4のような、LaをドーピングしたNaTaO3光触媒は、非常に高い活性を示し、水から、水素と酸素をそれぞれ、500 mL h-1,250 mL h-1で生成します(400 W高圧水銀灯を使用)。ここをクリックすると、そのときの様子を動画でみることができます。しかし、この光触媒は310 nm以下の紫外光しか吸収しないため、太陽光照射での活性を期待できません。

効率よく太陽光を利用できる光触媒を開発するには、光触媒のバンドギャップを狭くして長波長の光を利用できるようにすることが重要です。そのためには、次に示す3つの手法が挙げられます。
(1)バンドギャップの大きい光触媒への遷移金属ドーピング
(2)価電子帯制御
(3)固溶体形成
(1)遷移金属ドーピング
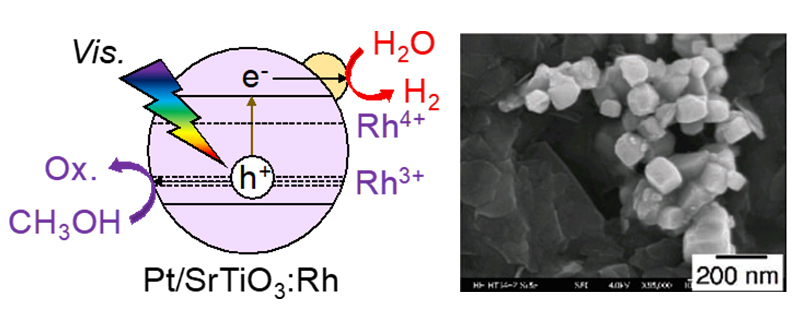
当研究室では、バンドギャップの大きい光触媒に金属イオンをドーピングすることで、バンドギャップ内に新しい準位を形成し、長波長の光を利用できる光触媒を開発してきました。特に、図5に示すようなRhドープSrTiO3光触媒は、可視光に応答して、還元剤存在下で高い水素活性を示します。
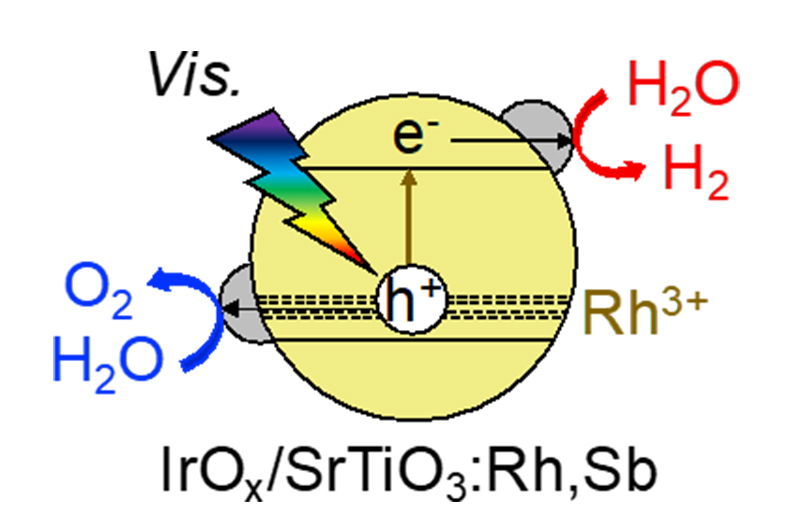
また、図6に示すように、IrOx助触媒を担持したRhおよびSbドープSrTiO3金属酸化物光触媒は、可視光水分解活性を示すことも見いだしました。さらに、Ir助触媒を担持したIrドープSrTiO3光触媒は、800 nmまでの光に応答して還元剤存在下で水素活性を示すことも見いだしました。
(2)価電子帯制御
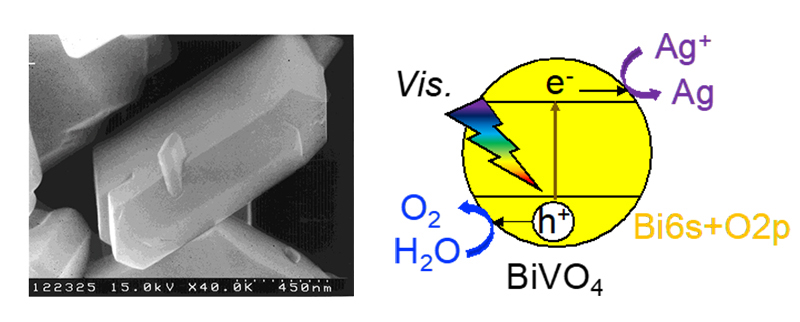
バンドギャップの広い光触媒の価電子帯に代わって、他の元素によって価電子帯を形成し、バンドギャップを狭くする方法です。当研究室では、BiVO4やAgVO3,SnNb2O6などを開発してきました。特に、図7に示すBiVO4は酸化剤存在下で可視光に応答して効率よく酸素を生成します。
また、Rh0.5Cr1.5O3助触媒を担持したAgTaO3光触媒は紫外光照射下ではあるものの、高い水分解活性を示すことを見いだしました。ここをクリックすると、そのときの様子を動画でみることができます。
(3)固溶体形成
固溶体を形成することでも、バンドギャップを狭くすることができます。当研究室では、可視光を照射すると、還元剤存在下において効率よく水素を生成できる、CuInS2,AgInS2およびZnSを組み合わせた光触媒を開発しました(図8)。特に、黒色光触媒であるCuInS2,AgInS2およびZnSを組み合わせた光触媒は830 nmまでの光に応答して水素を発生させることができます。ここをクリックすると、その時の様子を動画で見ることができます。

新規Z-スキーム系の開発
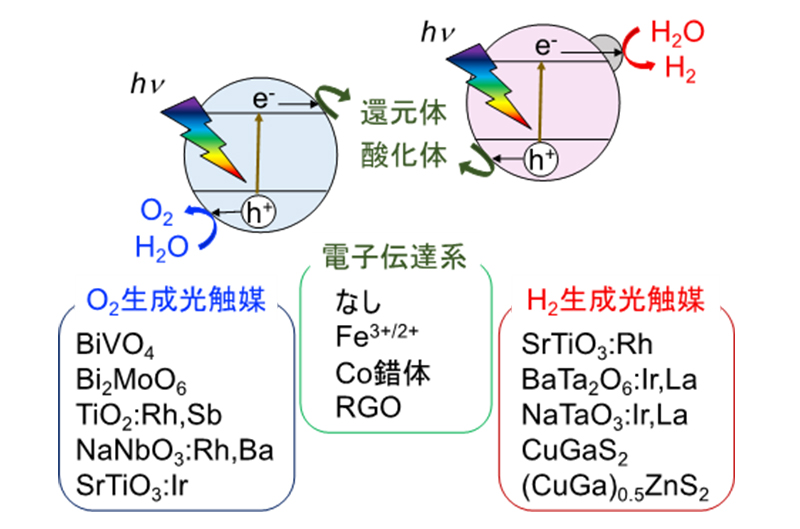
当研究室では、植物の光合成メカニズムである二段階光励起(Z-スキーム)を模倣して、水素生成光触媒および酸素生成光触媒を組み合わせたZ-スキーム型光触媒系の研究も行っています。図9に、そのZスキーム型光触媒系の反応メカニズムを示します。酸素生成光触媒上では、励起電子により電子伝達系の酸化体が還元体に還元され、正孔により水が酸化されて酸素が生成します。一方、水素生成光触媒上では、正孔により還元体が酸化され、励起電子により助触媒上で水を還元して水素が生成します。そして、電子伝達系は消費されることなくレドックスを繰り返すことで、全体では水分解が進行します。また、太陽光照射下において水分解反応の進行を確認しています。さらに近年では、電子伝達剤を使わないZスキーム系についても研究を行っていま 吶
参考文献
- R. Konta, T. Ishii, H. Kato, A. Kudo, J. Phys. Chem. B 2004, 108, 8992.
- R. Asai, H. Nemoto, Q. Jia, K. Saito, A. Iwase, A. Kudo, Chem. Commun. 2014, 50, 2543.
- S. Suzuki, A. Iwase, A. Kudo, Chem. Commun. 2018, 54, 10606.
- A. Kudo, K. Omori, H. Kato, J. Am. Chem. Soc. 1999, 121, 11459.
- R. Konta, H. Kato, H. Kobayashi, A. Kudo, Phys. Chem. Chem. Phys. 2003, 5, 3061.
- Y. Hosogi, H. Kato, and A. Kudo, J. Mater. Chem. 2008, 18, 647.
- Y. Hosogi, K. Tanabe, H. Kato, H. Kobayashi, A. Kudo, Chem. Lett. 2004, 33, 28.
- K. Watanabe, A. Iwase, A. Kudo, Chem. Sci. 2020, 11, 2330.
- I. Tsuji, H. Kato, A. Kudo, Angew. Chem. Int. Ed. 2005, 44, 3565.
- H. Kato, M. Hori, R. Konta, Y. Shimodaira, A. Kudo, Chem. Lett. 2004, 33, 1348.
- Y. Sasaki, H. Nemoto, K. Saito, A. Kudo, J. Phys. Chem. C 2009, 113, 17536.
- Y. Sasaki, H. Kato, A. Kudo, J. Am. Chem. Soc. 2013, 135, 5441.
- A. Kudo, S. Yoshino, T. Tsuchiya, Y. Udagawa, Y. Takahashi, M. Yamaguchi, I. Ogasawara, H. Matsumoto, A. Iwase, Faraday Discuss. 2019, 215, 313.
- H. Kato, M. Hori, R. Konta, Y. Shimodaira, A. Kudo, Chem. Lett. 2004, 33, 1348.
- A. Iwase, A. Kudo, Chem. Commun. 2017, 53, 6156.
- K. Iwashina, A. Iwase, Y. H. Ng, R. Amal, A. Kudo, J. Am. Chem. Soc. 2015, 137, 604.
- T. Kato, Y. Hakari, S. Ikeda, Q. Jia, A. Iwase, A. Kudo, J. Phys. Chem. Lett. 2015, 6, 1042.
